Konfigurasi elektron unsur transisi periode 4.
Jika kamu mencari artikel konfigurasi elektron unsur transisi periode 4 terbaru, berarti kamu sudah berada di blog yang benar. Yuk langsung saja kita simak ulasan konfigurasi elektron unsur transisi periode 4 berikut ini.
 Unsur Transisi Periode Ke 4 From slideshare.net
Unsur Transisi Periode Ke 4 From slideshare.net
Unsur transisi bersifat logam. 2 18 4 C. Tak memiliki satu elektron pada subkulit d. Konfigurasi Elektron Unsur Transisi Nama Unsur Lambang Nomor Atom Struktur Elektron Golongan Skandium Sc 21 Ar 3 d 1 4 s 2 IIIB 3 Titanium Ti 22 Ar 3 d 2 4 s 2 IVB 4 Vanadium V 23 Ar 3 d 3 4 s 2 VB 5 Kromium Cr 24 Ar 3 d 5 4 s 1 VIB 6 Mangan Mg 25 Ar 3 d 5 4 s 2 VIIB 7 Besi Fe 26 Ar 3 d 6 4 s 2 VIIIB 8 Kobalt Co 27 Ar 3 d 7 4.
Unsur-Unsur Transisi Periode Keempat.
Subkulit d -nya terisi penuh. Admin dari blog Berbagai Unsur 2019 juga mengumpulkan gambar-gambar lainnya terkait konfigurasi elektron unsur transisi periode 4 dibawah ini. 6 Dapat membentuk ion kompleks. Senyawa-senyawa unsur transisi di alam ternyata mempunyai bilangan oksidasi lebih dari satu. PUSAT PERBUKUAN PUSAT PERBUKUAN Departemen Pendidikan Nasional Departemen Pendidikan Nasional.
 Source: slideplayer.info
Source: slideplayer.info
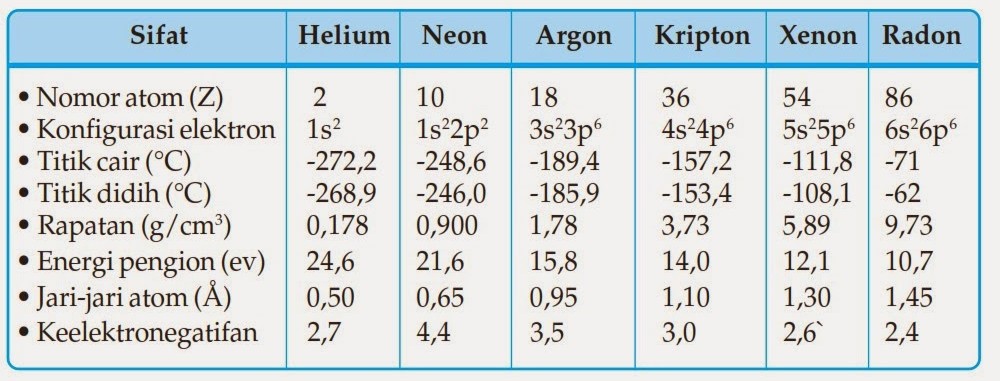
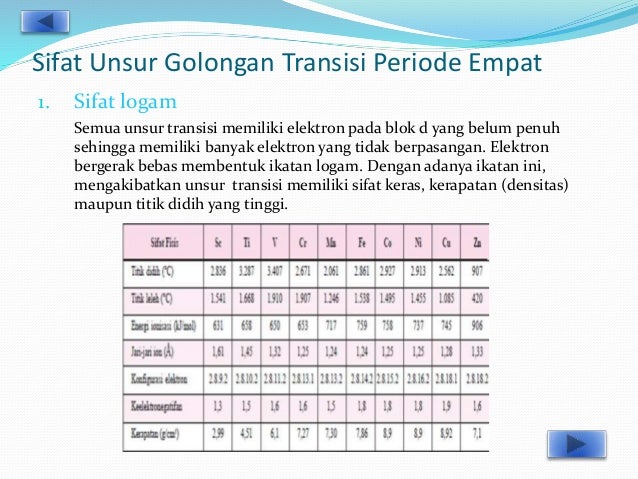
Unsur-unsur transisi termasuk periode keempat dari sifat kimia dan fisis bersifat logam. Kecuali unsur Cr dan Cu semua unsur transisi periode keempat mempunyai elektron pada kulit terluar 4s 2 sedangkan pada Cr dan Cu adalah 4s 1. Konfigurasi Elektron Kecuali unsur Cr dan Cu Semua unsur transisi periode keempat mempunyai elektron pada kulit terluar 4s2 sedangkan pada Cr dan Cu terdapat pada subkulit 4s1. PUSAT PERBUKUAN PUSAT PERBUKUAN Departemen Pendidikan Nasional Departemen Pendidikan Nasional. Transisis peride 4 dalam SPU.
Dari konfigurasi elektronnya dapatlah dipahami mengapa unsur transisi periode keempat tidak mengikuti pola pergeseran sifat seperti pada periode ketiga.
Unsur Transisi Periode Ke 4 Keempat Sifat Konfigurasi Elektron Titik Didih dan Leleh Jari-jari Atom Logam Magnet Bilangan Oksidasi Warna Ion Kimia 1 Penamaan Ligan a Beberapa ligan diberi nama khusus. Suatu atom terletak pada golongan III A periode 4 maka konfigurasi elektron unsur tersebut adalah. NH3 amin H2O aqua NO nitrosil CO karbonil b. Hal itu tidak lain karena elektron valensi unsur transisi tidak mengisi subkulit p melainkan subkulit d Juga dapat dimengerti mengapa unsur transisi terletak antara golongan IIA dan IIIA yaitu karena subkulit d selalu.
 Source: slidetodoc.com
Source: slidetodoc.com
Sip berarti periode 4 itu yang kulitnya ada 4 golongan B yang polanya ada s sama dnya. 7 Mempunyai beberapa tingkat oksidasi. Senyawa dari unsur transisi periode keempat yang mengandung ion Sc 3 dan Ti 4 tidak berwarna. 2 8 18 3 E.
 Source: brainly.co.id
Source: brainly.co.id
Unsur unsur transisi periode keempat. Sip berarti periode 4 itu yang kulitnya ada 4 golongan B yang polanya ada s sama dnya. Hal itu tidak lain karena elektron valensi unsur transisi tidak mengisi subkulit p melainkan subkulit d Juga dapat dimengerti mengapa unsur transisi terletak antara golongan IIA dan IIIA yaitu karena subkulit d selalu. Konfigurasi Elektron Kecuali unsur Cr dan Cu Semua unsur transisi periode keempat mempunyai elektron pada kulit terluar 4s2 sedangkan pada Cr dan Cu terdapat pada subkulit 4s1.
 Source: cute766.info
Source: cute766.info
3 Rapuh tetapi keras. Hal itu tidak lain karena elektron valensi unsur transisi tidak mengisi subkulit p melainkan subkulit d Juga dapat dimengerti mengapa unsur transisi terletak antara golongan IIA dan IIIA yaitu karena subkulit d selalu. 2 18 4 C. Hal ini menyebabkan unsur transisi periode keempat memiliki beberapa sifat khas yang tidak dimiliki oleh unsur-unsur golongan utama seperti sifat magnetik warna ion aktivitas katalitik serta kemampuan membentuk senyawa.
4 Mempunyai senyawa berwaran. 2 18 8 3. Terus ada apa aja sih di periode 4 golongan B. Lihat pola konfigurasi diatas n nya itu lho periode.
3 Rapuh tetapi keras.
Unsur unsur transisi periode keempat. Senyawa-senyawa unsur transisi di alam ternyata mempunyai bilangan oksidasi lebih dari satu. 2 18 8 3. 1 Mempunyai titik lebur rendah. Di antara berbagai sifat unsur berikut.
 Source: slideplayer.info
Source: slideplayer.info
Transisi periode keempat mempunyai keelektronegatifan yang rendah jadi energi ionisasi dan keelektropositifannya rendah. Hal ini menyebabkan unsur transisi periode keempat memiliki beberapa sifat khas yang tidak dimiliki oleh unsur-unsur golongan utama seperti sifat magnetik warna ion aktivitas katalitik serta kemampuan membentuk senyawa. Potensial energi unsur transisi periode 4 yang berharga negatif kecuali Cu menyatakan bahwa unsur unsur transisi ini bersifat reduktor. Hal ini disebabkan tingkat energi orbital s dan orbital d tidak berbeda jauh sehingga memungkinkan elektron-elektron pada kedua orbital itu digunakan melalui pembentukan orbital hibrida sp3d2. Jika nomor massa atom tersebut 127 maka jumlah neutron unsur tersebut adalah.
Transisis peride 4 dalam SPU. Konfigurasi Elektron Kecuali unsur Cr dan Cu Semua unsur transisi periode keempat mempunyai elektron pada kulit terluar 4s2 sedangkan pada Cr dan Cu terdapat pada subkulit 4s1. 4 Mempunyai senyawa berwaran. Jadi junlah kulit pada suatu konfigurasi elektron menenjukkan periode unsur tersebut.
Subkulit d -nya terisi penuh.
7 Mempunyai beberapa tingkat oksidasi. 2 8 8 3 D. 2 8 18 3 E. Transisi periode keempat mempunyai keelektronegatifan yang rendah jadi energi ionisasi dan keelektropositifannya rendah.

Konfigurasi Elektron Unsur Transisi Nama Unsur Lambang Nomor Atom Struktur Elektron Golongan Skandium Sc 21 Ar 3 d 1 4 s 2 IIIB 3 Titanium Ti 22 Ar 3 d 2 4 s 2 IVB 4 Vanadium V 23 Ar 3 d 3 4 s 2 VB 5 Kromium Cr 24 Ar 3 d 5 4 s 1 VIB 6 Mangan Mg 25 Ar 3 d 5 4 s 2 VIIB 7 Besi Fe 26 Ar 3 d 6 4 s 2 VIIIB 8 Kobalt Co 27 Ar 3 d 7 4. Sifat reduktornya menyebabkan unsur-unsur transisi dapat bereaksi dengan unsur-unsur nonlogam seperti oksigen belerang dan halogen. Jadi junlah kulit pada suatu konfigurasi elektron menenjukkan periode unsur tersebut. 5 Menggunakan subkulit s untuk berikatan.
 Source: slideshare.net
Source: slideshare.net
Sifat reduktornya menyebabkan unsur-unsur transisi dapat bereaksi dengan unsur-unsur nonlogam seperti oksigen belerang dan halogen. Jadi junlah kulit pada suatu konfigurasi elektron menenjukkan periode unsur tersebut. 2 18 8 3. Kecuali unsur Cr dan Cu semua unsur transisi periode keempat mempunyai elektron pada kulit terluar 4s 2 sedangkan pada Cr dan Cu adalah 4s 1.
 Source: materikimia.com
Source: materikimia.com
Admin dari blog Berbagai Unsur 2019 juga mengumpulkan gambar-gambar lainnya terkait konfigurasi elektron unsur transisi periode 4 dibawah ini. Senyawa dari unsur transisi periode keempat yang mengandung ion Sc 3 dan Ti 4 tidak berwarna. Jadi junlah kulit pada suatu konfigurasi elektron menenjukkan periode unsur tersebut. Transisis peride 4 dalam SPU.
Transisi periode keempat mempunyai keelektronegatifan yang rendah jadi energi ionisasi dan keelektropositifannya rendah.
Dari konfigurasi elektronnya dapatlah dipahami mengapa unsur transisi periode keempat tidak mengikuti pola pergeseran sifat seperti pada periode ketiga. Kecuali unsur Cr dan Cu semua unsur transisi periode keempat mempunyai elektron pada kulit terluar 4s 2 sedangkan pada Cr dan Cu adalah 4s 1. Senyawa dari unsur transisi periode keempat yang mengandung ion Sc 3 dan Ti 4 tidak berwarna. Jadi junlah kulit pada suatu konfigurasi elektron menenjukkan periode unsur tersebut. 1 Mempunyai titik lebur rendah.

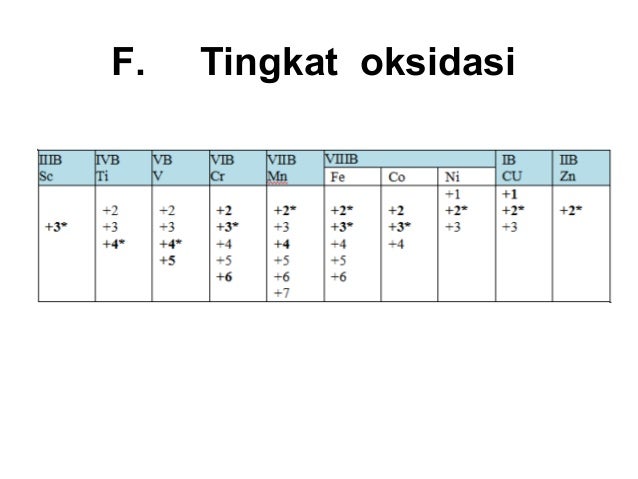
Senyawa-senyawa unsur transisi di alam ternyata mempunyai bilangan oksidasi lebih dari satu. 2 8 18 3 E. Admin dari blog Berbagai Unsur 2019 juga mengumpulkan gambar-gambar lainnya terkait konfigurasi elektron unsur transisi periode 4 dibawah ini. 7 Mempunyai beberapa tingkat oksidasi. Biloks yang bermacam-macam membuat transisi termasuk periode keempat bersifat ionik.
Kecuali unsur Cr dan Cu semua unsur transisi periode keempat mempunyai elektron pada kulit terluar 4s 2 sedangkan pada Cr dan Cu adalah 4s 1.
Hal ini disebabkan tingkat energi orbital s dan orbital d tidak berbeda jauh sehingga memungkinkan elektron-elektron pada kedua orbital itu digunakan melalui pembentukan orbital hibrida sp3d2. Umumnya unsur-unsur transisi periode keempat memiliki biloks lebih dari satu. Dari konfigurasi elektronnya dapatlah dipahami mengapa unsur transisi periode keempat tidak mengikuti pola pergeseran sifat seperti pada periode ketiga. Jadi junlah kulit pada suatu konfigurasi elektron menenjukkan periode unsur tersebut.
 Source: chemistry35.blogspot.com
Source: chemistry35.blogspot.com
Hal itu tidak lain karena elektron valensi unsur transisi tidak mengisi subkulit p melainkan subkulit d Juga dapat dimengerti mengapa unsur transisi terletak antara golongan IIA dan IIIA yaitu karena subkulit d selalu. Inilah pembahasan lengkap terkait konfigurasi elektron unsur transisi periode 4. Lihat pola konfigurasi diatas n nya itu lho periode. Tak memiliki satu elektron pada subkulit d.
 Source: slidetodoc.com
Source: slidetodoc.com
2 18 8 3. Transisis peride 4 dalam SPU. 2 8 4 B. Admin dari blog Berbagai Unsur 2019 juga mengumpulkan gambar-gambar lainnya terkait konfigurasi elektron unsur transisi periode 4 dibawah ini.
 Source: slideplayer.info
Source: slideplayer.info
Soal 10 Suatu unsur terletak pada golongan VIIA periode 5. NH3 amin H2O aqua NO nitrosil CO karbonil b. Unsur-Unsur Transisi Periode Keempat. Senyawa dari unsur transisi periode keempat yang mengandung ion Sc 3 dan Ti 4 tidak berwarna.
Suatu atom terletak pada golongan III A periode 4 maka konfigurasi elektron unsur tersebut adalah.
6 Dapat membentuk ion kompleks. Soal 10 Suatu unsur terletak pada golongan VIIA periode 5. Transisis peride 4 dalam SPU. UNSUR TRANSISI PERIODE KEEMPAT. Sip berarti periode 4 itu yang kulitnya ada 4 golongan B yang polanya ada s sama dnya.
 Source: slideshare.net
Source: slideshare.net
Suatu atom terletak pada golongan III A periode 4 maka konfigurasi elektron unsur tersebut adalah. Tak memiliki satu elektron pada subkulit d. PUSAT PERBUKUAN PUSAT PERBUKUAN Departemen Pendidikan Nasional Departemen Pendidikan Nasional. 2 8 8 3 D. Transisis peride 4 dalam SPU.
Biloks unsur-unsur transisi periode keempat ditunjukkan pada Tabel 43.
Sifat reduktornya menyebabkan unsur-unsur transisi dapat bereaksi dengan unsur-unsur nonlogam seperti oksigen belerang dan halogen. Biloks yang bermacam-macam membuat transisi termasuk periode keempat bersifat ionik. 2 8 4 B. Sifat reduktornya menyebabkan unsur-unsur transisi dapat bereaksi dengan unsur-unsur nonlogam seperti oksigen belerang dan halogen.
 Source: usaha321.net
Source: usaha321.net
2 8 18 3 E. 2 Untuk menyebut. Hal ini menyebabkan unsur transisi periode keempat memiliki beberapa sifat khas yang tidak dimiliki oleh unsur-unsur golongan utama seperti sifat magnetik warna ion aktivitas katalitik serta kemampuan membentuk senyawa. 3 Rapuh tetapi keras. Sifat reduktornya menyebabkan unsur-unsur transisi dapat bereaksi dengan unsur-unsur nonlogam seperti oksigen belerang dan halogen.
 Source: slidetodoc.com
Source: slidetodoc.com
7 Mempunyai beberapa tingkat oksidasi. 6 Dapat membentuk ion kompleks. Unsur-unsur transisi termasuk periode keempat dari sifat kimia dan fisis bersifat logam. Di antara berbagai sifat unsur berikut. Senyawa dari unsur transisi periode keempat yang mengandung ion Sc 3 dan Ti 4 tidak berwarna.
 Source: slideplayer.info
Source: slideplayer.info
2 18 4 C. UNSUR TRANSISI PERIODE KEEMPAT. Potensial energi unsur transisi periode 4 yang berharga negatif kecuali Cu menyatakan bahwa unsur unsur transisi ini bersifat reduktor. 2 8 4 B. Konfigurasi Elektron Unsur Transisi Nama Unsur Lambang Nomor Atom Struktur Elektron Golongan Skandium Sc 21 Ar 3 d 1 4 s 2 IIIB 3 Titanium Ti 22 Ar 3 d 2 4 s 2 IVB 4 Vanadium V 23 Ar 3 d 3 4 s 2 VB 5 Kromium Cr 24 Ar 3 d 5 4 s 1 VIB 6 Mangan Mg 25 Ar 3 d 5 4 s 2 VIIB 7 Besi Fe 26 Ar 3 d 6 4 s 2 VIIIB 8 Kobalt Co 27 Ar 3 d 7 4.
Situs ini adalah komunitas terbuka bagi pengguna untuk membagikan apa yang mereka cari di internet, semua konten atau gambar di situs web ini hanya untuk penggunaan pribadi, sangat dilarang untuk menggunakan artikel ini untuk tujuan komersial, jika Anda adalah penulisnya dan menemukan gambar ini dibagikan tanpa izin Anda, silakan ajukan laporan DMCA kepada Kami.
Jika Anda menemukan situs ini bagus, tolong dukung kami dengan membagikan postingan ini ke akun media sosial seperti Facebook, Instagram dan sebagainya atau bisa juga bookmark halaman blog ini dengan judul konfigurasi elektron unsur transisi periode 4 dengan menggunakan Ctrl + D untuk perangkat laptop dengan sistem operasi Windows atau Command + D untuk laptop dengan sistem operasi Apple. Jika Anda menggunakan smartphone, Anda juga dapat menggunakan menu laci dari browser yang Anda gunakan. Baik itu sistem operasi Windows, Mac, iOS, atau Android, Anda tetap dapat menandai situs web ini.





